2024年2月���,醫(yī)學(xué)部卡爾森國(guó)際腫瘤中心朱衛(wèi)國(guó)特聘教授團(tuán)隊(duì)在《Cell Reports》雜志上發(fā)表題為“The ARID1A-METTL3-m6A axis ensures effective RNase H1-mediated resolution of R-loops and genome stability”的研究論文���,揭示了R-loop中RNA發(fā)生的m6A甲基化修飾對(duì)于RNase H識(shí)別R-loop并驅(qū)動(dòng)R-Loop清除起到十分關(guān)鍵的作用。醫(yī)學(xué)部助理教授張俊���,研究生陳鳳為本研究共同第一作者��,朱衛(wèi)國(guó)特聘教授為通訊作者�����。

R-Loop是新轉(zhuǎn)錄生成的RNA鏈與DNA模板鏈形成的三鏈結(jié)構(gòu)�����,這種結(jié)構(gòu)在生物學(xué)中具有重要的功能��,但R-Loop在特定基因組位點(diǎn)的過(guò)度累積會(huì)引發(fā)基因組的不穩(wěn)定性�����。細(xì)胞內(nèi)存在多種機(jī)制防范R-Loop的過(guò)度積累�����,其中RNaseH被公認(rèn)為降解R-Loop的關(guān)鍵分子�。然而�����,目前人們尚不清楚R-Loop是如何被RNase H精確地識(shí)別和分解��,并最終達(dá)到維持基因組穩(wěn)定性的目的�����。
本研究首先證實(shí)了RNase H1RNase H1更傾向結(jié)合帶有m6A甲基化修飾的R-Loop����,并推動(dòng)R-Loop的分解以促進(jìn)DSB的DNA末端切除,從而確?��;蚪M的穩(wěn)定性���。機(jī)制上�����,該團(tuán)隊(duì)鑒定出ARID1A在響應(yīng)DNA損傷應(yīng)激時(shí)快速識(shí)別R-Loop并進(jìn)一步招募RNA甲基轉(zhuǎn)移酶METTL3/14���,從而驅(qū)動(dòng)R-LoopRNA發(fā)生m6A修飾。功能研究顯示ARID1A及METTL3的缺失會(huì)導(dǎo)致R-Loop積累����,同時(shí)ARID1A-METTL3信號(hào)軸缺陷的細(xì)胞對(duì)基因毒性療法更加敏感。鑒于異常表達(dá)的ARID1A與腫瘤患者對(duì)基因毒性療法的耐藥性有關(guān)���,這些發(fā)現(xiàn)為探索針對(duì)ARID1A異常表達(dá)癌癥的治療提供了潛在新策略(具體工作模式圖如下)��。
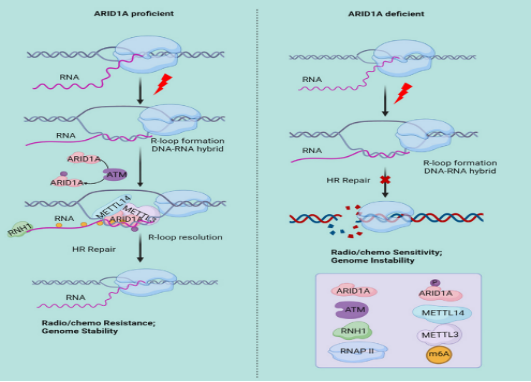
本研究得到國(guó)家自然科學(xué)基金�����,廣東省自然科學(xué)基金以及深圳市醫(yī)學(xué)研究基金等項(xiàng)目的資助���。
原文鏈接:https://www.sciencedirect.com/science/article/pii/S2211124724001074
(來(lái)源 深圳大學(xué)醫(yī)學(xué)部)





